1. Einleitung
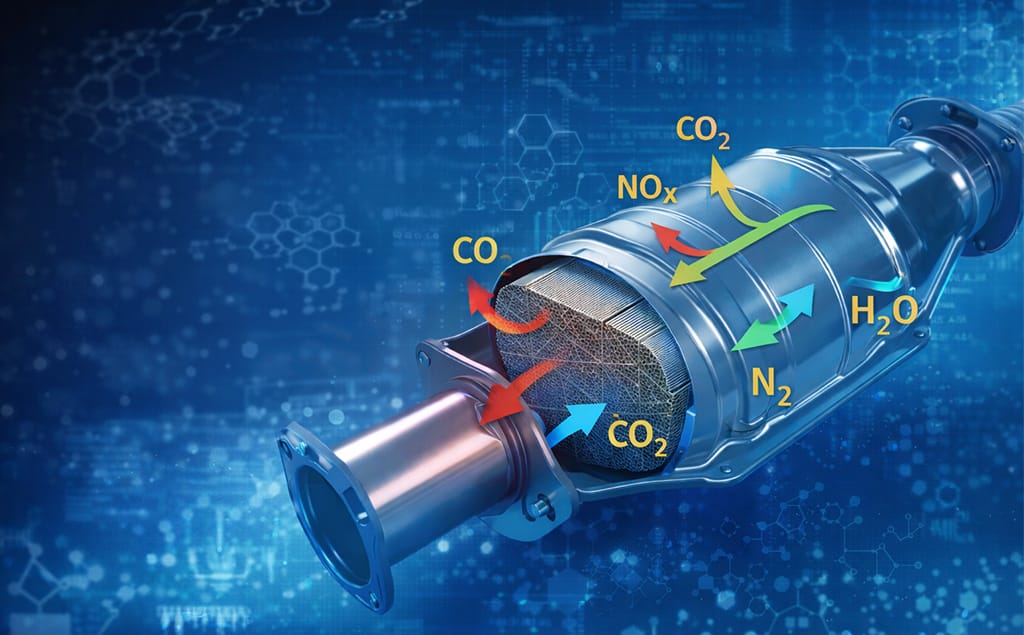
Katalysatoren sind unverzichtbare Komponenten moderner Fahrzeuge mit Verbrennungsmotor und dienen als primäre Abgasnachbehandlungstechnologie zur Reduzierung schädlicher Abgasemissionen. Ihre entscheidende Rolle besteht darin, giftige Schadstoffe – wie unverbrannte Kohlenwasserstoffe (HC), Kohlenmonoxid (CO) und Stickoxide (NOx) – in weniger schädliche Substanzen wie Wasserdampf, Kohlendioxid und Stickstoffgas umzuwandeln. 10Dieser Bericht befasst sich mit den grundlegenden wissenschaftlichen Mechanismen, durch die verschiedene Abgaskomponenten und Betriebsbedingungen die Leistung und Lebensdauer von Katalysatoren beeinträchtigen. Wir untersuchen die komplexen chemischen und physikalischen Prozesse, die bei verschiedenen Katalysatorarchitekturen zur Deaktivierung führen, und vermitteln ein umfassendes Verständnis dieser komplexen Wechselwirkungen.
2. Katalysatorarchitekturen und Funktionsprinzipien
Katalysatoren sind hochentwickelte chemische Reaktoren, die spezifische Redoxreaktionen ermöglichen. Ihre Kernstruktur besteht typischerweise aus einem keramischen (Cordierit) oder metallischen (Fecralloy) Wabenmonolithsubstrat, das eine große geometrische Oberfläche für den katalytischen Washcoat bietet. 37Dieser Washcoat, eine poröse Schicht, die üblicherweise aus Metalloxiden mit großer Oberfläche wie Gamma-Aluminiumoxid (γ-Al2O3), Siliciumdioxid (SiO2), Titandioxid (TiO2), Ceroxid (CeO2) und Zirkoniumdioxid (ZrO2) besteht, ist entscheidend für die Verteilung der aktiven katalytischen Materialien 40Die Washcoat-Dicke liegt typischerweise zwischen 20 und 40 µm, was einer Beladung von etwa 100 g/dm33 auf 200 cpsi (Zellen pro Quadratzoll) Substraten und bis zu 200 g/dm33 auf 400 cpsi Substraten entspricht. 57Die Wahl des Substrats und des Washcoat-Materials beeinflusst maßgeblich die thermische Stabilität, die mechanische Festigkeit und die Gesamtleistung des Katalysators 37.
Je nach Motortyp und Emissionszielen kommen unterschiedliche Katalysatortypen zum Einsatz:
2.1. Zweiwege-Katalysatoren
Zweiwegekatalysatoren werden hauptsächlich bei Dieselmotoren eingesetzt und konzentrieren sich auf die Oxidation von Kohlenwasserstoffen und Kohlenmonoxid 10Sie enthalten typischerweise Platin (Pt) und/oder Palladium (Pd) als aktive Edelmetalle.
2.2 Dreiwegekatalysatoren (TWCs)
TWCs sind der Standard für Benzinmotoren und sollen gleichzeitig drei Hauptschadstoffe reduzieren: Stickoxide (NOx), Kohlenmonoxid (CO) und unverbrannte Kohlenwasserstoffe (HC). 4Diese gleichzeitige Umwandlung wird durch ein empfindliches Gleichgewicht von Oxidations- und Reduktionsreaktionen erreicht, was erfordert, dass der Motor innerhalb eines engen stöchiometrischen Luft-Kraftstoff-Verhältnisfensters (A/F) (λ = 1) arbeitet, typischerweise zwischen 14,6 und 14,8 für Benzin 5.
Die aktiven Materialien in TWCs sind überwiegend Edelmetalle:
- Platin (Pt) Und Palladium (Pd) katalysieren hauptsächlich die Oxidation von CO und Kohlenwasserstoffen 1Die Oxidation von Kohlenwasserstoffen wie Propan (C3H8), Propen (C3H6) und Methan (CH4) wird als ähnlich der von CO angesehen. 1Die Aktivierungsenergien für die HC-Oxidation an Pd/Rh- und Pt/Pd/Rh-Katalysatoren liegen zwischen 105 und 125 kJ/mol, wobei die Methanoxidation eine besondere Herausforderung darstellt. 1.
- Rhodium (Rh) ist entscheidend für die Reduzierung von Stickoxiden 1. Rhodium-aktive Stellen erleichtern die Schwächung der NO-Bindung in NO, was zur Bildung von N2 führt 2.
Die wichtigsten chemischen Reaktionen, die in einem TWC ablaufen, sind:
- NOx-Reduktion: 2NO + 2CO → N₂ + 2CO₂ 3
- CO-Oxidation: 2CO + O₂ → 2CO₂ 3
- Kohlenwasserstoffoxidation: 2C₂H₆ + 7O₂ → 4CO₂ + 6H₂O 3
Nichtedle Metalloxide, insbesondere Ceroxid (CeO2), oft in Form eines CeO2-ZrO2-Mischoxids, spielen eine wichtige Rolle als Sauerstoffspeicherkomponenten (OSC). 1Diese Sauerstoffspeicherkapazität hilft dabei, Schwankungen im Luft-Kraftstoff-Verhältnis abzupuffern, das „Katalysatorfenster“ zu erweitern und eine hohe Umwandlungseffizienz auch bei transientem Motorbetrieb aufrechtzuerhalten. 5. So entwickelte Monolithos Catalysts & Recycling Ltd. PROMETHEUS, einen TWC-Katalysator mit Cu-, Pd- und Rh-Nanopartikeln auf einem CeO2-ZrO2-Mischoxid mit hohem OSC, was die Bedeutung dieser Mischoxide unterstreicht. 1.
2.3. Diesel-/Mager-NOx-Katalysatoren
Dieselmotoren arbeiten mit mageren Kraftstoffgemischen (Sauerstoffüberschuss), was die NOx-Reduktion für herkömmliche TWCs zu einer Herausforderung macht. Es kommen spezielle Systeme zum Einsatz:
- Dieseloxidationskatalysatoren (DOCs): Diese werden hauptsächlich zur Oxidation von CO und Kohlenwasserstoffen, einschließlich der löslichen organischen Fraktion (SOF) von Partikeln, und zur Oxidation von Stickoxid (NO) zu Stickstoffdioxid (NO2) verwendet. 10Das NO2 wird dann in nachgelagerten Komponenten wie Dieselpartikelfiltern verwendet.
- Dieselpartikelfilter (DPF): DPFs dienen dazu, Partikel (Ruß und Asche) aus Dieselabgasen physikalisch abzufangen. Sie bestehen typischerweise aus porösen Keramikmaterialien. Die Rußablagerung auf DPFs erfolgt in mehreren Stufen: Tiefenablagerung, Partikelbaumwachstum, Partikelbaumverbindung und Bildung einer Rußkuchenschicht. 28Die Rußkuchenschicht kann eine Dicke von 20-50 Mikrometern erreichen 28.
- Systeme zur selektiven katalytischen Reduktion (SCR): SCR-Systeme reduzieren die NOx-Emissionen durch die Einspritzung eines Reduktionsmittels, typischerweise Harnstoff (der sich zu Ammoniak, NH3, zersetzt), in den Abgasstrom vor einem Katalysator. Das Ammoniak reagiert dann selektiv mit NOx über einem Katalysator, meist einem zeolithbasierten Material, zu N2 und H2O. Die NOx-Umwandlungseffizienz in SCR-Systemen wird von der Katalysatortemperatur, der Gasgeschwindigkeit und dem NH3/NOx-Verhältnis beeinflusst. 48.
Die Gesamteffizienz von Katalysatoren wird von Faktoren wie Zelldichte, Wandstärke und der geometrischen Oberfläche des Substrats beeinflusst 38Eine höhere Zelldichte verbessert im Allgemeinen die Leistung durch Vergrößerung der Stoffaustauschfläche, erhöht aber auch den Druckabfall 38.
3. Abgaskomponenten: Reaktanten, Gifte und Promotoren
Abgas ist ein komplexes Gemisch aus Komponenten, von denen einige für die Umwandlung durch den Katalysator vorgesehen sind (Reaktanten), während andere seine Leistung stark beeinträchtigen (Gifte) oder in einigen Fällen seine Aktivität steigern können (Promotoren).
3.1. Reaktanten
Die primären Zielschadstoffe für die katalytische Umwandlung sind:
- Unverbrannte Kohlenwasserstoffe (HCs): Entsteht durch unvollständige Kraftstoffverbrennung.
- Kohlenmonoxid (CO): Ein Produkt unvollständiger Verbrennung.
- Stickoxide (NOx): Entstehen bei hohen Temperaturen während der Verbrennung vor allem NO und NO2.
3.2. Gifte
Katalysatorvergiftung ist die Deaktivierung eines Katalysators durch chemische Mittel, im Unterschied zu thermischer Zersetzung oder physikalischer Beschädigung 6Gifte binden typischerweise chemisch an die aktiven Stellen des Katalysators oder reagieren mit ihnen, wodurch deren Verfügbarkeit verringert und die Diffusionsdistanz für Reaktantenmoleküle vergrößert wird 6Dies führt zu einem Anstieg der Anspringtemperatur und einer Verringerung der maximalen Umwandlungseffizienz 7Eine Vergiftung kann reversibel oder irreversibel sein, wobei die Reversibilität bei höheren Temperaturen in einer reduzierenden Umgebung oft verstärkt wird. 8.
Zu den wichtigsten Katalysatorgiften zählen:
- Blei (Pb): Historisch gesehen war verbleites Benzin eine Hauptquelle für Bleivergiftungen. Blei, in Form von elementarem Blei, Blei(II)-oxid, Blei(II)-chlorid und Blei(II)-bromid, bildet Legierungen mit den Edelmetallen oder überzieht die Katalysatoroberfläche und verhindert so den Kontakt mit Abgasen. 610Eine Ablagerung von nur 0,5 % des Katalysatorgewichts kann zu einem Rückgang der Umwandlungseffizienz um 50 % führen 7.
- Schwefel (S): Schwefelverbindungen (SO2, SO3, H2S und verschiedene Sulfate) kommen natürlicherweise in Kraftstoffen und Schmiermitteln auf Erdölbasis vor und adsorbieren auf der Katalysatoroberfläche, was sich insbesondere auf Palladium (Pd) auswirkt. 7SO2 kann zu SO3 oxidiert und im Katalysator gespeichert werden 7Eine Schwefelvergiftung verringert sowohl die Light-Off- als auch die Warm-Up-Aktivität und erhöht die Light-Off-Temperatur deutlich. 7. Beispielsweise kann Kraftstoff mit hohem Schwefelgehalt (575 ppm) die Anspringtemperatur im Vergleich zu Kraftstoff mit niedrigem Schwefelgehalt (40 ppm) drastisch erhöhen. 7.
- Phosphor (P): Phosphorverbindungen sind ein häufiger Bestandteil von Schmieröladditiven, insbesondere Zinkdithiophosphat (ZDDP). Sie können Phosphate (z. B. Cer-, Zirkonium-, Aluminium- und Titanphosphate) und Zinkpyrophosphat bilden. 7Diese Verbindungen interagieren mit Washcoat-Komponenten wie Al2O3 und CeO2 und bilden eine Glasur, die die Katalysatoroberfläche versiegelt und den Gasdurchgang einschränkt 7. Eine Phosphorvergiftung ist oft ausgeprägter als die alleinige hydrothermale Alterung und betrifft in erster Linie die Oxidkomponenten und nicht die Edelmetalle 11.
- Zink (Zn): Zink stammt ebenfalls aus Schmierölzusätzen wie ZDDP und wandelt sich während der Verbrennung in Oxide um. Dies trägt zur Bildung einer Glasur auf der Katalysatoroberfläche bei und verringert die Effizienz durch die Abdeckung aktiver Stellen. 7.
- Silizium (Si): Ursachen sind Kühlmittellecks, verunreinigte Kraftstoffe (insbesondere unsachgemäß recyceltes Methanol oder Ethanol in Biokraftstoffen) und Silikondichtstoffe 7. Siliziumdioxid (SiO2) kann die Schutzhülle von Sauerstoffsensoren verstopfen, die Gasdiffusion einschränken und zu einer falschen Regelung des Luft-Kraftstoff-Gemischs führen, was wiederum zu unruhigem Motorleerlauf, hohem Kraftstoffverbrauch, erhöhten Emissionen und Schäden am Katalysator führt. 7Es kann sich auch direkt auf der Katalysatoroberfläche ablagern.
- Asche: Nicht brennbare Rückstände aus der Verbrennung von Kraftstoffen und Schmierölen sowie Asche können sich auf der Katalysatoroberfläche ansammeln, aktive Stellen physisch blockieren und zur Maskierung und zum Druckabfall beitragen. 40.
3.3. Veranstalter
Bestimmte Komponenten oder Zusatzstoffe können die Aktivität oder Haltbarkeit des Katalysators verbessern:
- Ceroxid (CeO2) und Ceroxid-Zirkonoxid (CeO2-ZrO2): Diese Mischoxide werden häufig als Sauerstoffspeichermittel eingesetzt und verbessern die Fähigkeit des Katalysators, vorübergehende Schwankungen des Luft-Kraftstoff-Verhältnisses zu bewältigen. 1Ceroxid fördert außerdem die Reduzierbarkeit und stabilisiert Edelmetallkatalysatoren in einem dispergierten Zustand, wodurch das Sintern bei hohen Temperaturen durch die Bildung oxidierter Pt-O-Ce-Bindungen verhindert wird 24.
- Kalzium (Ca): Forschungsergebnisse deuten darauf hin, dass die Zugabe von Kalzium zu einem mit Phosphor vergifteten Katalysator eine regenerierende Wirkung haben kann, was auf sein Potenzial als Förderer zur Abschwächung der Phosphordeaktivierung hindeutet. 11.
4. Chemische Vergiftung: Mechanismen der Deaktivierung aktiver Zentren
Eine chemische Vergiftung ist ein kritischer Abbauprozess, der zur irreversiblen oder semireversiblen Deaktivierung der aktiven Zentren des Katalysators führt. Dieser Abschnitt beschreibt die Mechanismen der wichtigsten Gifte auf atomarer Ebene.
4.1. Schwefelvergiftung
Schwefelverbindungen, vor allem H2S und SO2, sind starke Katalysatorgifte. Der Mechanismus beruht auf der starken Adsorption und Reaktion von Schwefelspezies mit den aktiven Metallzentren, wodurch diese effektiv blockiert werden und Reaktantenmoleküle den Zugang zur katalytischen Oberfläche verhindern. 17.
- Adsorption und Reaktion: H2S reagiert direkt mit aktiven Metallstellen und führt zur Deaktivierung 17. SO2, particularly in diesel exhaust, interacts with copper-chabazite (Cu-CHA) catalysts used for NOx reduction. Studies have shown that SO2 reacts with the [Cu2II(NH3)4O2]2+ complex, forming CuI species and a sulfated CuII complex that accumulates within the zeolite pores 18. Röntgenabsorptionsspektroskopie (XAS) bestätigt die Bildung von sulfatierten Komponenten (SO42-) 18.
- Auswirkungen auf die Leistung: Eine Schwefelvergiftung verringert die Ammoniak-Speicherkapazität (NH3) des Katalysators erheblich, beeinträchtigt die vorübergehende NOx-Reduktionseffizienz und führt zu einem vorzeitigen Ammoniakaustritt 19Höhere SO2-Konzentrationen beschleunigen diese Deaktivierung 19.
- Reversibilität und Regeneration: Einige Schwefelvergiftungen können durch die Entfernung von H2S aus dem Einsatzmaterial oder durch die Durchleitung eines Inertgases durch das Katalysatorbett rückgängig gemacht werden, was auf ein Gleichgewicht zwischen gasförmigem und adsorbiertem H2S hinweist. 20Die Bindungsenergie einiger sulfatierter Spezies (SO42-) bleibt jedoch nach der Regeneration weitgehend unverändert, insbesondere bei solchen, die unter hohen Schwefelkonzentrationen gebildet wurden, was ihre Entfernung erschwert. 18Schwefel-Ammoniak-Verbindungen können bei 500 °C zersetzt werden, wodurch die NOx-Reduktionsleistung teilweise wiederhergestellt wird, während Schwefel-Kupfer-Verbindungen höhere Temperaturen (600 °C) für nur eine teilweise Wiederherstellung erfordern. 19. Hochtemperaturoxidation kann eine wirksame Regenerationsmethode sein 17Die Schwere der SO2-Vergiftung unterstreicht die Notwendigkeit von Dieselkraftstoff mit extrem niedrigem Schwefelgehalt, um die Katalysatordeaktivierung in Dieselabgassystemen zu mildern 18.
- Konkurrenz zur Kokerei: Während Verkokung (Kohlenstoffablagerung) ein weiterer Deaktivierungsmechanismus ist, insbesondere bei Kohlenwasserstoffreaktionen, kann das Vorhandensein von Cer im Katalysator dessen Widerstandsfähigkeit gegen Kohlenstoffablagerung erhöhen, wodurch eine Schwefelvergiftung in solchen Fällen zu einem bedeutenderen Deaktivierungsfaktor wird. 17.
4.2. Phosphorvergiftung
Phosphor, hauptsächlich aus Schmierölzusätzen wie ZDDP, deaktiviert Katalysatoren, indem er eine physikalische Barriere bildet und chemisch mit dem Washcoat interagiert.
- Glasurbildung: Phosphorverbindungen wie Phosphate und Zinkpyrophosphat bilden eine glasartige Schicht oder Glasur auf der Katalysatoroberfläche 7Diese Glasur versiegelt die Passagen innerhalb des Washcoats und verhindert, dass Abgase die aktiven Stellen erreichen 7.
- Wechselwirkung mit Washcoat: Phosphorverbindungen interagieren chemisch mit Washcoat-Komponenten wie Aluminiumoxid (Al2O3) und Ceroxid (CeO2) und bilden stabile Phosphate (z. B. Cer-, Zirkonium-, Aluminium- und Titanphosphate). 7Diese Wechselwirkung betrifft in erster Linie die Oxidkomponenten des Katalysators, anstatt die Edelmetalle direkt zu vergiften. 11Die Bildung dieser stabilen Verbindungen kann die Porenstruktur des Washcoats verändern und seine Oberfläche verringern, was die katalytische Aktivität weiter beeinträchtigt.
4.3. Bleivergiftung
Blei, das ursprünglich aus verbleitem Benzin stammt, ist ein äußerst schädliches und weitgehend irreversibles Katalysatorgift.
- Oberflächenbeschichtung und Legierung: Bleiverbindungen lagern sich bei der Verbrennung auf der Katalysatoroberfläche ab und bilden eine nicht poröse Beschichtung, die die aktiven Stellen physikalisch blockiert 10Darüber hinaus kann Blei mit den Edelmetallen (Pt, Pd, Rh) legieren, wodurch deren elektronische Struktur grundlegend verändert wird und sie katalytisch inaktiv werden. 10Dieser Mechanismus ist besonders schwerwiegend und führt zu einer schnellen und erheblichen Verschlechterung der Katalysatorleistung 7.
4.4. Silizium- und Zinkvergiftung
- Silizium: Siliziumverbindungen, die häufig aus Kühlmittellecks oder verunreinigten Kraftstoffen stammen, können sich als Kieselsäure (SiO2) auf der Katalysatoroberfläche ablagern oder Sauerstoffsensoren verstopfen. 7. Silica-Ablagerungen auf dem Katalysator wirken wie eine physikalische Barriere, maskieren aktive Stellen und reduzieren die effektive Oberfläche. Verstopfte Sauerstoffsensoren führen zu einer ungenauen Regelung des Luft-Kraftstoff-Verhältnisses, was zu einem suboptimalen Motorlauf führt und andere Abbaumechanismen verschlimmern kann. 7.
- Zink: Ähnlich wie Phosphor bildet Zink aus Ölzusätzen bei der Verbrennung Oxide, die zur Glasurbildung auf der Katalysatoroberfläche beitragen und so die Effizienz weiter verringern, indem sie aktive Stellen bedecken. 7.
Zusammenfassend lässt sich sagen, dass chemische Vergiftungsmechanismen die Bildung starker chemischer Bindungen oder physikalischer Barrieren an den aktiven Stellen und dem Washcoat des Katalysators beinhalten, was zu einer dauerhaften Verringerung der katalytischen Aktivität und der Umwandlungseffizienz führt. Die Reversibilität der Vergiftung hängt stark vom spezifischen Gift, seiner chemischen Form und den Betriebsbedingungen ab.
5. Thermische Degradation (Sintern): Einfluss hoher Temperaturen auf die Katalysatorstruktur
Thermal degradation, particularly sintering, is a major cause of catalytic converter deactivation, especially at temperatures exceeding 500°C [L.5.3]. This process involves the irreversible loss of active surface area due to the agglomeration of noble metal particles and the structural collapse of the washcoat.
5.1. Edelmetallsintern
Sintern bezeichnet das Wachstum von Edelmetallpartikeln (Pt, Pd, Rh) bei erhöhten Temperaturen, was zu einer Verringerung der gesamten aktiven Oberfläche führt, die für katalytische Reaktionen zur Verfügung steht. 22.
- Mechanismus: Edelmetallpartikel, die zunächst stark auf dem Washcoat verteilt sind, können über die Trägeroberfläche wandern und miteinander verschmelzen (Partikelmigration und -koaleszenz) oder größere Partikel können auf Kosten kleinerer Partikel wachsen (Ostwald-Reifung). 24Dieser Prozess wird durch hohe Temperaturen und das Vorhandensein von Wasserdampf beschleunigt 24.
- Anfälligkeit von Platin: Platin (Pt) ist besonders anfällig für Sinterung, insbesondere in oxidierenden Atmosphären 22Die Unterdrückung der Platinsinterung ist entscheidend für die Haltbarkeit des Katalysators 22.
- Einfluss des Trägermaterials: Die Wahl des Trägermaterials beeinflusst das Sinterverhalten maßgeblich. Ceroxid-basierte Oxide (CeO2) sind wirksame Träger für Pt, da sie starke Pt-O-Ce-Bindungen bilden können, die als „Anker“ wirken und das Sintern von Pt unterdrücken. 23Die Stärke dieser Wechselwirkung korreliert mit der Elektronendichte des Sauerstoffs im Trägeroxid 23Umgekehrt sind Zirkonoxid-basierte Oxide (ZrO2) besser für Rh geeignet, insbesondere unter oxidierenden Bedingungen, da Rh im Oxidzustand stärker mit Oxidträgern interagiert. 22Eine optimierte Katalysatorkonfiguration beinhaltet oft Pt auf Ceroxid-basiertem Oxid und Rh auf Zirkonoxid-basiertem Oxid, um das Sintern beider Metalle zu unterdrücken 22.
- Die Rolle des Wassers: Wasser (H2O) kann das Sintern erheblich beeinflussen. Bei Temperaturen über 500 °C wird der hemmende Effekt von Wasser auf die katalytische Aktivität vernachlässigbar, und das Sintern von Pd wird deutlicher. 24In Abwesenheit von H2O wird die Ostwald-Reifung begünstigt, aber in Gegenwart von H2O kann die Bildung von Silanolgruppen (Si-OH) die Migration und Koaleszenz von Pd auf SiO2-Trägern begünstigen 24.
5.2. Struktureller Zusammenbruch des Washcoats
Der Washcoat selbst kann einer thermischen Zersetzung unterliegen, was zu einer Verringerung seiner großen Oberfläche und seines Porenvolumens führt.
- Mechanismus: Sustained high temperatures can cause the porous washcoat structure to collapse, reducing the available surface area for noble metal dispersion and catalytic reactions [L.5.3]. This is often associated with phase transformations or crystallite growth within the washcoat material.
- Auswirkungen: Eine Verringerung der Washcoat-Oberfläche führt direkt zu einer Verringerung der Anzahl verfügbarer aktiver Stellen, selbst wenn die Edelmetalle selbst nicht so stark sintern. Dies beeinträchtigt auch die Sauerstoffspeicherkapazität von Materialien wie Ceroxid und verschlechtert die Katalysatorleistung weiter.
Das Zusammenspiel zwischen Edelmetallsinterung und Washcoat-Degradation ist komplex. Starke Metall-Träger-Wechselwirkungen, wie die Pt-O-Ce-Bindungen, sind entscheidend für die Stabilisierung der Edelmetalle und verhindern deren Agglomeration. Dadurch wird die thermische Stabilität des Katalysators erhöht. 24. Die Kalzinierungsvorbehandlung von Trägermaterialien kann auch die Edelmetalldispersion und die Sinterbeständigkeit beeinflussen 26.
6. Physikalische Degradation: Erosion, Maskierung und mechanische Beschädigung
Neben der chemischen und thermischen Zersetzung sind Katalysatoren auch anfällig für physikalische Schäden durch Abgaskomponenten und mechanische Belastungen.
6.1. Rußmaskierung
Ruß, vor allem aus der Dieselverbrennung, kann die aktiven Stellen des Katalysators physisch blockieren, ein Phänomen, das als Maskierung bezeichnet wird. 27.
- Mechanismus: Rußpartikel lagern sich auf der Katalysatoroberfläche ab und bilden eine physikalische Barriere, die die Diffusion der Abgase zu den Katalysatoren behindert und so die Umwandlungseffizienz verringert. 27Bei Dieselpartikelfiltern (DPFs) verläuft die Rußablagerung in verschiedenen Phasen: Tiefenablagerung, Partikelbaumwachstum, Partikelbaumverbindung und schließlich die Bildung einer Rußkuchenschicht 28Diese Kuchenschicht kann eine Dicke von 20-50 Mikrometern erreichen 28.
- Auswirkungen auf SCR-Katalysatoren: Rußbeladung auf SCR-beschichteten Filtern erhöht den Ammoniakschlupf (NH3) während der Adsorption und verringert die NOx-Umwandlung 29. Die Wirkung von Ruß auf die katalytische Aktivität ist in erster Linie physikalischer Natur und erzeugt Diffusionsbarrieren, nicht aber chemische Wechselwirkungen. 29In Filtern mit integrierten SCR-Katalysatoren kann die Reaktion von NO2 mit Ruß sogar mit der gewünschten schnellen SCR-Reaktion konkurrieren 29.
- Rußeigenschaften: Die Wirksamkeit der Rußoxidation wird durch die Rußzusammensetzung und Mikrostruktur beeinflusst, die je nach Kraftstoff, Schmieröl, Motortyp und Betriebsbedingungen variieren. 27Echter Motorruß hat oft eine „schalenartige“ Struktur mit einem kristallisierten graphitartigen Kern, was zu höheren Zündtemperaturen im Vergleich zu amorphem Kohlenstoff führt 34. Enger Kontakt zwischen Ruß und Katalysator verbessert die Reaktionsraten, aber die realen DPF-Bedingungen ähneln oft einem losen Kontakt 30.
6.2. Washcoat-Erosion
Der kontinuierliche Strom heißer Abgase, insbesondere solcher, die Partikel enthalten, kann zur physischen Erosion des Washcoats führen.
- Mechanismus: Substraterosion erfordert das Vorhandensein von Partikeln im Abgasstrom 35Das Ausmaß der Erosion hängt von Faktoren wie Partikelgeschwindigkeit, Größe, Morphologie und Aufprallwinkel ab 35Ein ungleichmäßiger Abgasstrom kann auch zu einer lokalen Erosion der Substratoberfläche beitragen und so die aktive Oberfläche verringern. 27.
- Faktoren, die die Erosion beeinflussen: Erosion wird im Allgemeinen bei höheren Temperaturen reduziert 35. Die zunehmende Verwendung von Substraten mit hoher Zelldichte und dünnen Wänden (z. B. 600/4, 600/3, 900/2), um strenge Emissionsstandards zu erfüllen und die Kosten für Edelmetalle zu senken, wirft auch Bedenken hinsichtlich ihrer Anfälligkeit für Erosion auf 35.
- Schadensbegrenzung: Zum Schutz des Katalysators werden Technologien zur Reduzierung der Mattenmontageerosion eingesetzt, wie z. B. Drahtgeflechtdichtungen, Versteifungen, Kantenbehandlung mit Silica-Gewebe und polykristalline Kantendichtungen. 33.
6.3. Mechanische Schäden
Katalysatoren sind im Fahrzeugbetrieb erheblichen mechanischen Belastungen ausgesetzt, die zu Strukturschäden führen können.
- Vibrationen: Motor- und Straßenvibrationen können dazu führen, dass der Keramikmonolith Risse oder Brüche bekommt, insbesondere an den Befestigungspunkten oder aufgrund unzureichender Verpackung.
- Thermoschock: Schnelle Temperaturänderungen, wie sie beispielsweise bei Kaltstarts oder plötzlichen Motorabschaltungen auftreten, können thermische Spannungen verursachen, die zu Rissen im Keramiksubstrat führen. 47Die eng gekoppelte Platzierung der Katalysatoren, die für ein schnelleres Anspringen ausgelegt sind, verstärkt die Bedenken hinsichtlich struktureller Schäden aufgrund schwerer thermischer und mechanischer Bedingungen 35.
- Substratkollaps: Starke mechanische oder thermische Belastungen können zum vollständigen Zusammenbruch des Substrats führen, den Abgasstrom blockieren und erhebliche Leistungseinbußen beim Motor verursachen. 53Hohe Washcoat-Beladungen können zwar die aktive Oberfläche vergrößern, aber die physikalische Haltbarkeit moderner Katalysatoren beeinträchtigen, insbesondere bei motornahen Anwendungen. 61.
Diese physikalischen Abbaumechanismen reduzieren direkt die wirksame katalytische Oberfläche, behindern den Stofftransport von Schadstoffen und können zu einem katastrophalen Ausfall des Katalysators führen.
7. Einfluss der Betriebsbedingungen auf die Degradationsraten
Die Betriebsbedingungen des Motors spielen eine entscheidende Rolle bei der Beschleunigung oder Abschwächung der Rate chemischer Vergiftungen, thermischer Zersetzung und physischer Schäden.
7.1. Normaler stöchiometrischer Betrieb
Bei Dreiwegekatalysatoren ist die Einhaltung eines präzisen stöchiometrischen Luft-Kraftstoff-Verhältnisses (A/F) (λ=1) für eine optimale Leistung entscheidend. 4Abweichungen von diesem engen „Katalysatorfenster“ können zu einer unvollständigen Umwandlung von Schadstoffen führen und in einigen Fällen zur Verschlechterung des Katalysators beitragen. Beispielsweise weisen magere Gemische hohe NOx- und niedrige CO/HC-Werte auf, während fette Gemische hohe CO/HC- und niedrige NOx-Werte aufweisen. 5. Eine präzise Regelung des Luft-Kraftstoff-Verhältnisses, die oft durch die Rückmeldung eines Sauerstoffsensors erreicht wird, ist unerlässlich 5.
7.2. Fehlzündungen
Fehlzündungen im Motor, bei denen das Luft-Kraftstoff-Gemisch in einem oder mehreren Zylindern nicht richtig verbrennt, sind für Katalysatoren äußerst schädlich. 52.
- Überladung mit unverbranntem Kraftstoff: Durch Fehlzündungen gelangen große Mengen unverbrannten Kraftstoffs in die Abgasanlage und anschließend in den Katalysator. 52. Katalysatoren sind nicht für so hohe Rohkraftstoffkonzentrationen ausgelegt 53.
- Überhitzung: Der unverbrannte Kraftstoff entzündet sich im Katalysator aufgrund der hohen Innentemperaturen (normaler Betriebsbereich: 1200–1600 °F). 53Diese Verbrennung im Konverter führt zu einer extremen Überhitzung, die möglicherweise 2000 °F übersteigt und den Konverter hellrot färbt 56.
- Strukturelle Schäden: Diese extreme Hitze kann die innere Struktur des Konverters schmelzen oder beschädigen, was zu Verstopfungen oder einem vollständigen Ausfall führen kann 53Das geschmolzene Material behindert den Abgasstrom und verschlechtert die Motorleistung und den Kraftstoffverbrauch zusätzlich. 53.
- Konsequenzen: Fehlzündungen können zu einem vorzeitigen Ausfall des Katalysators führen, was wiederum zu einer verringerten Fahrzeugleistung, einem höheren Kraftstoffverbrauch und erhöhten Emissionen führt. 53Zu den Symptomen zählen eine geringere Kraftstoffeffizienz, das Aufleuchten der Motorkontrollleuchte (Codes P0420 oder P0430), schlechte Beschleunigung, Leistungsverlust, Motorverzögerung, Abwürgen, Schwefelgeruch und übermäßige Hitzeentwicklung. 55.
- Ursachen für Fehlzündungen: Fehlzündungen können durch eine magere Verbrennung (zu viel Luft), undichte Einspritzdüsen oder sogar einen defekten Sauerstoffsensor verursacht werden, der ein fettes Luft-Kraftstoff-Gemisch verursacht. 56. Moderne Motormanagementsysteme sind darauf ausgelegt, Fehlzündungen frühzeitig zu erkennen und den Fahrer zu warnen 52. Eine rechtzeitige Wartung ist unerlässlich, um schwere Schäden zu vermeiden 53.
7.3. Längere Reich/Mager-Exkursionen
Während kurze Abweichungen durch die Sauerstoffspeicherkapazität ausgeglichen werden, kann ein längerer Betrieb außerhalb des stöchiometrischen Fensters den Abbau beschleunigen.
- Reichhaltige Bedingungen: Excess fuel can lead to carbon deposition (coking) on the catalyst surface, masking active sites and reducing efficiency [L.5.5]. It can also lead to the formation of metal carbonyls (e.g., Ni(CO)4) at lower temperatures and high CO partial pressures, causing catalyst loss [L.5.10].
- Magere Bedingungen: Überschüssiger Sauerstoff kann die Oxidation von Schwefelverbindungen zu stabileren Sulfaten fördern, die schwerer zu entfernen sind und zu einer irreversiblen Vergiftung beitragen. 18. Es kann auch das Sintern von Edelmetallen beschleunigen, insbesondere bei Platin 22.
7.4. Kaltstarts und vorübergehende Ereignisse
- Kaltstarts: During cold starts, the catalyst is below its light-off temperature, meaning it is ineffective at converting pollutants [L.5.1]. This period contributes significantly to overall emissions. The catalyst’s warm-up time is crucial for light-off 38.
- Vorübergehende Ereignisse: Schnelle Änderungen der Motorlast und -drehzahl führen zu Schwankungen in der Abgaszusammensetzung und -temperatur. Sauerstoffspeicherkomponenten helfen zwar, doch anhaltende oder starke Transienten können den Katalysator belasten, den thermischen Abbau beschleunigen und möglicherweise zu mechanischer Ermüdung führen.
7.5. Temperaturmanagement
The operating temperature of the catalyst is critical. While high temperatures accelerate sintering, a certain temperature is necessary for the catalytic reactions to occur efficiently. For instance, in biomass pyrolysis vapor upgrading, increasing catalyst temperature can counteract deactivation, but the rate of increase needs optimization [L.5.8]. An optimal operating temperature range exists for catalysts, balancing conversion efficiency and minimizing coke formation [L.5.11].
8. Folgen der Degradation: Leistungskennzahlen und Emissionsauswirkungen
Der Katalysatorabbau äußert sich in quantifizierbaren Leistungskennzahlen und wirkt sich direkt auf die Einhaltung der Emissionsvorschriften und die Gesamtfunktionalität des Fahrzeugs aus.
8.1. Reduzierte Umwandlungseffizienz
Die unmittelbarste Folge der Katalysatorzersetzung ist eine Verringerung seiner Fähigkeit, schädliche Schadstoffe in harmlose Substanzen umzuwandeln.
- Verlust aktiver Standorte: Chemical poisoning, thermal sintering, and physical masking all lead to a reduction in the number of available active sites on the catalyst surface [L.5.4][L.5.5][L.5.6]. This directly translates to fewer reaction pathways for pollutants.
- Schadstoffspezifische Auswirkungen:
- Kohlenwasserstoffe (HC) und Kohlenmonoxid (CO): Eine verringerte aktive Oberfläche bedeutet eine weniger effiziente Oxidation dieser Verbindungen.
- Stickoxide (NOx): Die Deaktivierung von Rhodiumstellen oder eine Vergiftung durch Schwefel kann die NOx-Reduktionsleistung erheblich beeinträchtigen 19.
- Faktoren, die die Konvertierung beeinflussen: Die Umwandlungseffizienz wird durch die Betriebsbedingungen des Fahrzeugs beeinflusst, einschließlich der Konzentration der Gasarten, der Temperatur und des Massenstroms am Katalysatoreinlass 39Auch die Washcoat-Formulierung spielt eine Rolle, da sie sich auf das Anspringverhalten und den Druckabfall auswirkt. 46Bei niedrigen Raumgeschwindigkeiten können keramische Substrate bessere Umwandlungen zeigen, während metallische Substrate aufgrund der größeren geometrischen Oberfläche bei hohen Raumgeschwindigkeiten eine bessere Leistung erbringen können. 39.
8.2. Erhöhte Light-Off-Temperatur (T50, T90)
Die Anspringtemperatur (T50 oder T90, die Temperatur, bei der 50 % bzw. 90 % eines Schadstoffs umgewandelt werden) ist ein entscheidender Indikator für die Katalysatorleistung.
- Erhöhung der Light-Off-Temperatur: Catalyst deactivation, whether due to poisoning, coking, or thermal degradation, invariably leads to an increase in the light-off temperature required for efficient pollutant conversion [L.5.1]. This means the catalyst takes longer to become effective after a cold start, leading to higher emissions during the warm-up phase.
- Mechanismus: The increase in light-off temperature is a direct result of the reduced active surface area and the diminished intrinsic activity of the catalyst. For instance, strong CO adsorption on catalytic sites can impede O2 adsorption at low CO conversions, resulting in U-shaped light-off curves [L.5.9]. Once CO desorbs, the reaction proceeds rapidly [L.5.9].
- Betriebsbedingungen des Motors: Light-off temperature varies with engine speed and torque due to changes in exhaust flow rate [L.5.2]. Light-off curves are highly dependent on reaction conditions, making extrapolation to other conditions (flow rates, catalyst amount, reactant concentrations) challenging [L.5.11].
8.3. Emissionsauswirkungen und Einhaltung
Die Folgen einer Verschlechterung wirken sich direkt auf die Fähigkeit eines Fahrzeugs aus, strenge Emissionsvorschriften einzuhalten.
- Erhöhte Abgasemissionen: Eine verringerte Umwandlungseffizienz und erhöhte Anspringtemperaturen führen dazu, dass mehr unverbrannte Kohlenwasserstoffe, Kohlenmonoxid und Stickoxide in die Atmosphäre freigesetzt werden, was zur Luftverschmutzung beiträgt.
- Nichtbestehen der Emissionsprüfungen: Fahrzeuge mit defekten Katalysatoren werden die vorgeschriebenen Abgastests wahrscheinlich nicht bestehen, was zu kostspieligen Reparaturen und möglichen rechtlichen Konsequenzen führen kann.
- Diagnose-Fehlercodes: Eine unzureichende Katalysatorleistung löst häufig Diagnosefehlercodes (DTCs) wie P0420 oder P0430 aus, die darauf hinweisen, dass die Leistung des Katalysators unter einem bestimmten Schwellenwert liegt. 53.
Im Wesentlichen beeinträchtigt die Katalysatorzersetzung den eigentlichen Zweck des Katalysators und führt zu Umweltschäden und Betriebsproblemen für das Fahrzeug.
9. Minderungsstrategien und zukünftige Katalysatortechnologien
Die Verschlechterung von Katalysatoren ist eine ständige Herausforderung im Automobilbau. Aktuelle und zukünftige Strategien konzentrieren sich auf die Verbesserung der Haltbarkeit, die Verbesserung der Katalysatorformulierungen und die Optimierung des Motormanagements.
9.1. Kraftstoff- und Schmierstoffqualität
- Kraftstoffe mit extrem niedrigem Schwefelgehalt: Der wirksamste Weg, einer Schwefelvergiftung vorzubeugen, ist die Verwendung von Kraftstoffen mit extrem niedrigem Schwefelgehalt 18Dadurch wird die Menge an Schwefelverbindungen, die in das Abgassystem gelangen, deutlich reduziert.
- Phosphor-/Zinkarme Öle: Durch die Reduzierung oder den Ersatz von Zinkdithiophosphat (ZDDP) in Schmierölen wird die Phosphor- und Zinkverunreinigung minimiert 7. Zinkersatzadditive können die notwendige Schmierung ohne die schädlichen Auswirkungen von ZDDP gewährleisten 15.
9.2. Motormanagement und Wartung
- Schnelle Fehlzündungskorrektur: Moderne Motormanagementsysteme sind darauf ausgelegt, Fehlzündungen frühzeitig zu erkennen 52. Durch die sofortige Behebung von Fehlzündungen, undichten Einspritzdüsen und Kühlmittellecks wird verhindert, dass übermäßig viel unverbrannter Kraftstoff, Öl und Kühlmittel in den Katalysator gelangt, wodurch eine starke Überhitzung und Beschädigung verhindert wird. 7.
- Präzise Regelung des Luft-Kraftstoff-Verhältnisses: Die Aufrechterhaltung des Luft-Kraftstoff-Verhältnisses des Motors innerhalb des optimalen stöchiometrischen Fensters für TWCs ist entscheidend für die Maximierung der Umwandlungseffizienz und die Minimierung von Bedingungen, die den Abbau beschleunigen 5.
- Adsorbentien: Die Verwendung fester Adsorbentien (z. B. Aluminiumoxid, Aktivkohle, Cordierit, Zeolith) zur Entfernung von Phosphorverbindungen aus der Kurbelgehäuseentlüftung und den Abgasrückführungsströmen kann den Katalysator vor einer Vergiftung schützen. 7.
9.3. Fortschrittliche Katalysatorformulierungen und Washcoat-Materialien
Umfangreiche Forschungs- und Entwicklungsarbeiten konzentrieren sich auf die Schaffung robusterer und effizienterer Katalysatoren.
- Verbesserte Washcoat-Materialien:
- Große Oberfläche und thermische Stabilität: Washcoat-Materialien wie Gamma-Aluminiumoxid (γ-Al2O3), Zeolithe, Siliciumdioxid (SiO2), Titandioxid (TiO2), Ceroxid (CeO2), Zirkoniumdioxid (ZrO2), Vanadiumoxid (V2O5) und Lanthanoxid (La2O3) werden kontinuierlich weiterentwickelt, um eine höhere spezifische Oberfläche (BET typischerweise 100-200 m22/g) und eine verbesserte thermische Stabilität zu erreichen. 57.
- Zusatzstoffe: Additive wie die pyrogene Kieselsäure AEROSIL von Evonik, die Kieselsäuredispersionen AERODISP und AEROPERL (pyrogene Kieselsäure, Titandioxid, Aluminiumoxide mit sphärischen Partikeln) werden verwendet, um Edelmetalle zu fixieren und die Stabilität der katalytischen Schicht zu verbessern. 58.
- Mehrschichtige Washcoats: Der Einsatz mehrschichtiger Washcoats ermöglicht unterschiedliche chemische Zusammensetzungen in jeder Schicht und optimiert so Leistung und Haltbarkeit. 57.
- Neuartige Katalysatorformulierungen:
- Optimierte Edelmetalldispersion: Die Strategien konzentrieren sich auf die Schaffung starker Metall-Träger-Wechselwirkungen (z. B. Pt-O-Ce-Bindungen), um Edelmetallpartikel zu verankern und das Sintern zu unterdrücken, was zu einer höheren katalytischen Aktivität und Haltbarkeit führt 23Eine optimierte Konfiguration beinhaltet Pt auf Ceroxid-basiertem Oxid und Rh auf Zirkonoxid-basiertem Oxid 22.
- Trimetallische und bimetallische Katalysatoren: Fortschrittliche metallische Katalysatorformulierungen, wie beispielsweise trimetallischer K6 (Pt:Pd:Rh) und bimetallischer K7 (Pd+Pd:Rh), sind darauf ausgelegt, die NOx-Reduktionseigenschaften von Pt:Rh mit der HC-Oxidationsaktivität von Pd zu kombinieren. Sie enthalten oft spezielle Katalysatorstrukturen mit optimierter Washcoat-Leistung für verbessertes Anspringen, thermische Stabilität und transiente Leistung. 59.
- Perowskite und Mischoxide: Die Erforschung komplexer Mischoxide und Perowskitstrukturen bietet das Potenzial für die Entwicklung von Katalysatoren mit hoher Aktivität und verbesserter Beständigkeit gegen Vergiftung und Sinterung, wodurch die Abhängigkeit von teuren Edelmetallen möglicherweise verringert wird.
9.4. Neuartige Substratdesigns
- Metallische Substrate: Metallische Substrate werden auf ihre Fähigkeit untersucht, Katalysatoren zu entwickeln, die bei niedrigen Abgastemperaturen effektiver sind und verbesserte Sauerstoffspeichereigenschaften in den Washcoats aufweisen. 59. Sie bieten auch Vorteile hinsichtlich der Werkzeugflexibilität und integrierter Häute zum Schweißen 37.
- Hohe Zelldichte und dünne Wände: Katalysatorträger mit höherer Zelldichte, geringerer Wandstärke, größerer Oberfläche und geringerer thermischer Masse sind für ein schnelleres Anspringen und eine höhere Umwandlungseffizienz wünschenswert 61. Hohe Washcoat-Beladungen bei diesen Designs können jedoch die physikalische Haltbarkeit beeinträchtigen 61.
- Anwendungen mit geschlossener Kupplung: Bei eng gekoppelten Konvertern sind die Optimierung der Substrat-/Washcoat-Interaktion, des geometrischen Designs und der Montagesysteme entscheidend für die Light-Off-Leistung und die FTP-Effizienz 61.
9.5. DPF-Regenerationsstrategien
Bei Dieselsystemen ist eine wirksame DPF-Regeneration der Schlüssel zur Verhinderung der Rußmaskierung.
- Passive Regeneration: Verwendet Katalysatoren, um die Rußoxidationstemperatur zu senken und so eine kontinuierliche Regeneration während des normalen Betriebs zu ermöglichen 42Die NO2-unterstützte Regeneration, bei der NO zu NO2 oxidiert wird, ist besonders effektiv, da NO2 ein stärkeres Oxidationsmittel für Kohlenstoff ist als Sauerstoff 43.
- Aktive Regeneration: Dazu gehört die Erhöhung der Abgastemperatur (z. B. durch Kraftstoffeinspritzung), um angesammelten Ruß zu verbrennen 42Eine erzwungene Regeneration kann notwendig sein, wenn der DPF zu stark verstopft ist 42.
- Auswirkungen auf SCR: Erhöhte Temperaturen während der DPF-Regeneration können die NOx-Umwandlungseffizienz in Motoren mit SCR-Nachbehandlung negativ beeinflussen 43.
9.6. Zukünftige Richtungen und Spekulationen
- Selbstheilende Katalysatoren (Spekulation): Das Konzept selbstheilender Katalysatormaterialien, die durch Vergiftung oder Sintern beschädigte aktive Zentren oder Washcoat-Strukturen reparieren können, befindet sich derzeit noch in der frühen Forschungsphase. Es birgt jedoch ein enormes Potenzial zur Verlängerung der Katalysatorlebensdauer. Mögliche Materialien sind Materialien, die aktive Komponenten freisetzen oder strukturelle Umstrukturierungen durchlaufen, um unter bestimmten Bedingungen die Funktionalität wiederherzustellen.
- Erweiterte Sensorintegration und KI/ML für vorausschauende Wartung (Spekulation): Die Integration hochentwickelterer In-situ-Sensoren, die den Katalysatorverschleiß in Echtzeit überwachen (z. B. aktive Oberfläche, spezifische Vergiftungsgrade), könnte eine hochpräzise, vorausschauende Wartung ermöglichen. Algorithmen des maschinellen Lernens könnten diese Sensordatenströme in Kombination mit Motorbetriebsparametern analysieren, um Katalysatorausfälle vorherzusagen, bevor sie sich auf die Emissionen auswirken. Dies ermöglicht proaktives Eingreifen statt reaktivem Austausch. Dies könnte auch die Regenerationszyklen von DPFs und SCRs optimieren.
- Biokraftstoffkompatibilität: Da Biokraftstoffe immer häufiger zum Einsatz kommen, ist es von entscheidender Bedeutung, die Auswirkungen neuer Schadstoffe (z. B. Silizium aus unsachgemäß recyceltem Ethanol) auf die Katalysatorvergiftung zu verstehen und zu mildern. 7.
- Nachhaltige Katalysatormaterialien: Das Streben nach Nachhaltigkeit wird weiterhin zu einer geringeren Abhängigkeit von Edelmetallen und zur Entwicklung häufiger vorkommender, kostengünstigerer und umweltfreundlicherer Katalysatormaterialien führen. 60.
The average catalyst life has already increased significantly from 2-3 years to 5-6 years due to advancements in catalyst preparation [L.5.12], highlighting the continuous progress in this field.
10. Fazit
Die Wirksamkeit und Langlebigkeit von Katalysatoren werden maßgeblich durch das komplexe Zusammenspiel zwischen Abgaszusammensetzung, Motorbetriebsbedingungen und der Werkstoffbeschaffenheit des Katalysators beeinflusst. Chemische Vergiftung, thermischer Abbau (Sintern) und physikalische Schäden (Maskierung, Erosion, mechanische Belastung) sind die Hauptursachen dafür, dass Abgaskomponenten die Katalysatorleistung beeinträchtigen. Jeder dieser Mechanismen führt zu einer Verringerung der aktiven Oberfläche und einer Erhöhung der Anspringtemperatur, was sich direkt auf die Einhaltung strenger Emissionsstandards auswirkt.
Das Verständnis der Wechselwirkungen von Giftstoffen wie Schwefel, Phosphor, Blei, Zink und Silizium mit Edelmetallen und Washcoat-Materialien auf atomarer Ebene ist entscheidend für die Entwicklung widerstandsfähigerer Katalysatoren. Ebenso ist die Minderung der Sinterung von Edelmetallen durch optimierte Trägermaterialien und starke Metall-Träger-Wechselwirkungen für die thermische Beständigkeit von größter Bedeutung. Der physikalische Abbau durch Partikel und mechanische Belastungen erfordert robuste Substratdesigns und effektive Regenerationsstrategien.
Kontinuierliche Fortschritte bei Washcoat-Materialien, Katalysatorformulierungen und intelligenten Motormanagementsystemen erweitern kontinuierlich die Grenzen der Katalysatorhaltbarkeit und -effizienz. Die Abgasreinigung der Zukunft wird voraussichtlich einen synergetischen Ansatz erfordern, der fortschrittliche Materialwissenschaft mit ausgefeilten Motor- und Abgasnachbehandlungssteuerungsstrategien kombiniert und möglicherweise Selbstheilungsfunktionen und KI-gesteuerte vorausschauende Wartung integriert, um sauberere Luft und nachhaltige Mobilität zu gewährleisten.