Introduzione
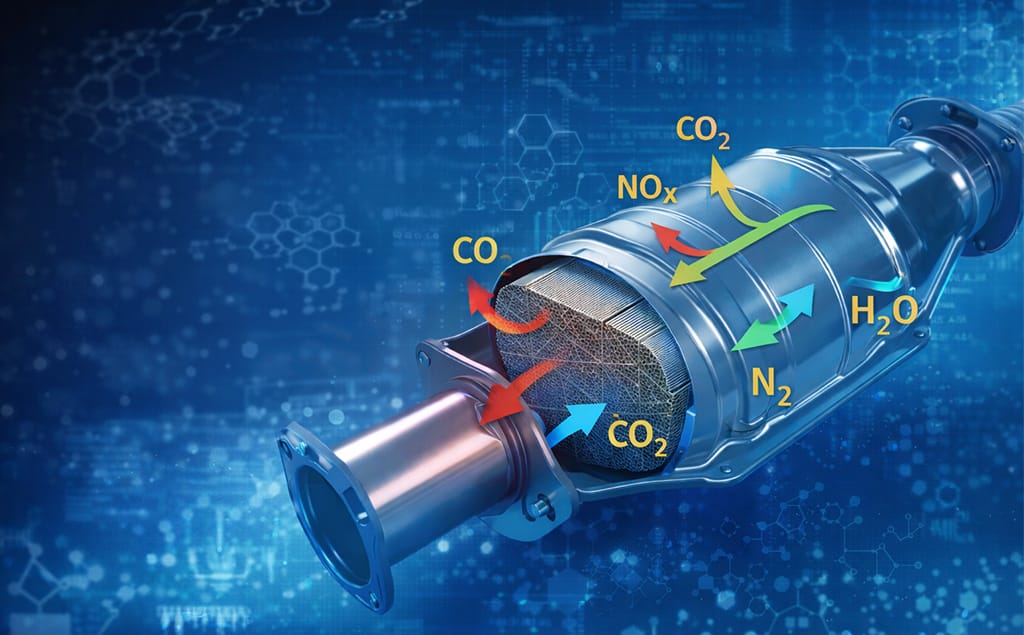
Ogni moderno veicolo a benzina contiene un notevole pezzo di ingegneria chimica nascosto nel suo sistema di scarico. Questo dispositivo, il convertitore catalitico a tre vie, ha un unico, cruciale scopo: neutralizzare gli inquinanti più nocivi prodotti da un motore a combustione interna. Senza di esso, le nostre città sarebbero soffocate dallo smog e la qualità dell'aria rappresenterebbe una minaccia significativa per la salute pubblica. Il processo di combustione del motore, sebbene potente, è imperfetto. Genera sottoprodotti tossici come monossido di carbonio, idrocarburi incombusti e ossidi di azoto. Il convertitore catalitico a tre vie funge da ultima linea di difesa. Trasforma questi gas pericolosi in sostanze innocue prima ancora che raggiungano il tubo di scarico. Questo articolo fornisce un'analisi scientifica e tecnica del convertitore catalitico a tre vie. Esamineremo la sua storia, i suoi complessi processi chimici, i suoi componenti fisici e le condizioni precise necessarie per il suo funzionamento efficace.
Capitolo 1: L'evoluzione dai convertitori bidirezionali a quelli tridirezionali
Il viaggio verso il moderno convertitore catalitico a tre vie L'iniziativa è nata da una crescente consapevolezza dell'inquinamento atmosferico. A metà del XX secolo, scienziati e autorità di regolamentazione hanno identificato i gas di scarico dei veicoli come una delle principali fonti di smog urbano. La prima importante risposta legislativa negli Stati Uniti è stata il Clean Air Act, che ha conferito all'Agenzia per la Protezione Ambientale (EPA) il potere di stabilire limiti rigorosi alle emissioni dei veicoli.
Il primo passo: convertitori di ossidazione bidirezionali
Le case automobilistiche risposero inizialmente con il convertitore catalitico "bidirezionale". Questi dispositivi apparvero per la prima volta su larga scala nel mercato statunitense sulla maggior parte dei veicoli del 1975. Il loro compito era quello di contrastare due dei tre principali inquinanti: il monossido di carbonio (CO) e gli idrocarburi incombusti (HC).
Questi primi convertitori funzionavano come catalizzatori di ossidazione. All'interno del dispositivo, l'ossigeno presente nel flusso di scarico reagiva con CO e HC. Questa reazione chimica, accelerata da catalizzatori come platino e palladio, li convertiva in due composti molto più sicuri: anidride carbonica (CO₂) e acqua (H₂O). Pur essendo efficaci in questo specifico compito, i convertitori bidirezionali non facevano nulla per contrastare il terzo principale inquinante: gli ossidi di azoto (NOx). Gli NOx sono un componente chiave nella formazione delle piogge acide e dell'ozono troposferico.
La soluzione completa: l'avvento del convertitore a tre vie
Con l'inasprimento delle normative, la necessità di una soluzione più completa divenne urgente. Gli ingegneri svilupparono il convertitore "a tre vie" per affrontare contemporaneamente tutte e tre le classi di inquinanti. Volvo fu un pioniere, introducendo i primi convertitori commerciali a tre vie sui suoi veicoli del 1977 per il mercato californiano, dove vigevano le leggi sulle emissioni più severe.
Entro l'anno modello 1981, le normative federali richiedevano significative riduzioni delle emissioni di NOx. Questo mandato ha reso di fatto il convertitore catalitico a tre vie Un componente standard ed essenziale su tutte le nuove auto a benzina negli Stati Uniti. Questa tecnologia ha rappresentato un importante passo avanti, poiché incorporava un secondo processo chimico, la riduzione, accanto all'ossidazione. Questa capacità a doppia azione è ciò che la rende "trivalente".
Confronto: convertitori catalitici a due vie e a tre vie
La distinzione tra queste due tecnologie è fondamentale. La tabella seguente ne illustra le principali differenze. I veicoli moderni utilizzano esclusivamente convertitori a tre vie per soddisfare gli standard globali sulle emissioni.
| Caratteristica | Convertitore catalitico bidirezionale | Convertitore catalitico a tre vie |
|---|---|---|
| Inquinanti trattati | Monossido di carbonio (CO), idrocarburi (HC) | Monossido di carbonio (CO), idrocarburi (HC), ossidi di azoto (NOx) |
| Processo chimico primario | Ossidazione | Ossidazione e riduzione |
| Metalli catalizzatori utilizzati | Platino (Pt), Palladio (Pd) | Platino (Pt), Palladio (Pd), Rodio (Rh) |
| Funzione primaria | Converte CO in CO₂ e HC in CO₂ + H₂O | Esegue le stesse reazioni di ossidazione più riduce NOx a N₂ |
| Applicazione moderna | Obsoleto nelle auto a benzina; utilizzato in alcune applicazioni diesel e a combustione magra | Di serie su quasi tutti i veicoli moderni a benzina |
Capitolo 2: La chimica di base di un convertitore catalitico a tre vie
UN convertitore catalitico a tre vie È essenzialmente un reattore chimico. Utilizza materiali specifici, noti come catalizzatori, per accelerare le reazioni chimiche senza essere consumati nel processo. Il nome "a tre vie" indica la sua capacità di promuovere tre trasformazioni chimiche simultanee. Queste reazioni sono raggruppate in due processi distinti: riduzione e ossidazione.
Questi due processi avvengono in fasi separate o su materiali catalizzatori diversi all'interno dell'alloggiamento del convertitore. Affinché entrambi funzionino in modo efficiente, la centralina del motore deve mantenere un equilibrio molto preciso tra carburante e aria.
La reazione di riduzione: neutralizzazione degli ossidi di azoto (NOx)
La prima fase di conversione è rivolta agli inquinanti più difficili da eliminare, gli ossidi di azoto (NOx). Questa famiglia di gas si forma quando azoto e ossigeno reagiscono in condizioni di alta pressione e alta temperatura all'interno dei cilindri di un motore.
Il catalizzatore di riduzione è responsabile della scomposizione degli NOx. Il rodio (Rh) è il metallo prezioso prescelto per questo compito. Ha la capacità unica di separare gli atomi di ossigeno dalle molecole di ossido di azoto. Questa reazione libera gli atomi di azoto, che poi si legano tra loro per formare azoto gassoso innocuo (N₂), il componente principale dell'aria che respiriamo.
- Reazione chimica: 2NOx → xO₂ + N₂
In questa reazione, il catalizzatore al rodio facilita la scomposizione degli NOx in ossigeno elementare e azoto gassoso stabile.
La reazione di ossidazione: pulizia di CO e HC
La seconda fase gestisce il monossido di carbonio (CO) e gli idrocarburi incombusti (HC). Il monossido di carbonio è un gas tossico derivante dalla combustione incompleta del carburante. Gli idrocarburi sono semplicemente particelle di carburante grezzo e incombusto.
Il catalizzatore di ossidazione utilizza l'ossigeno liberato durante la fase di riduzione, insieme a qualsiasi altro ossigeno disponibile nei gas di scarico, per convertire questi due inquinanti. Platino (Pt) e Palladio (Pd) sono i metalli principali utilizzati in questo processo. Promuovono reazioni che aggiungono ossigeno alle molecole di CO e HC.
- Ossidazione del monossido di carbonio: 2CO + O₂ → 2CO₂
- Ossidazione degli idrocarburi: CₓH₂ₓ₊₂ + [(3x+1)/2]O₂ → xCO₂ + (x+1)H₂O
Questo processo trasforma il tossico monossido di carbonio in anidride carbonica (CO₂) non tossica e converte gli idrocarburi inquinanti in anidride carbonica e vapore acqueo (H₂O).
Riepilogo delle trasformazioni chimiche
La tabella seguente riassume gli inquinanti in ingresso e i loro prodotti in uscita dopo il passaggio attraverso un convertitore catalitico a tre vie.
| Inquinante in ingresso | Formula chimica | Tipo di reazione | Catalizzatore metallico | Prodotto in uscita | Formula chimica |
|---|---|---|---|---|---|
| ossidi di azoto | NOx | Riduzione | Rodio (Rh) | Azoto gassoso | N₂ |
| monossido di carbonio | CO | Ossidazione | Platino (Pt), Palladio (Pd) | anidride carbonica | CO₂ |
| idrocarburi | HC | Ossidazione | Platino (Pt), Palladio (Pd) | Anidride carbonica e acqua | CO₂ e H₂O |
Capitolo 3: Anatomia di un convertitore catalitico a tre vie
Sebbene la chimica sia complessa, la struttura fisica di un convertitore è progettata per la massima efficienza e durata. È composta da tre componenti principali che lavorano all'unisono: il substrato, il washcoat e lo strato catalizzatore.
Il substrato: una fondazione di massima superficie
Il cuore del convertitore è il substrato. Si tratta di un monolite ceramico, tipicamente costituito da cordierite o talvolta da una struttura metallica. Non è un blocco solido, ma un'intricata struttura a nido d'ape. Questa struttura presenta migliaia di minuscoli canali paralleli.
Lo scopo del nido d'ape è massimizzare la superficie di contatto con i gas di scarico. Una superficie maggiore consente reazioni chimiche più efficienti e rapide in uno spazio fisico compatto. La densità di questi canali, misurata in celle per pollice quadrato (CPSI), può variare. Le applicazioni ad alte prestazioni possono utilizzare un CPSI più elevato per una migliore conversione, mentre i veicoli standard utilizzano un equilibrio tra efficienza e flusso.
Il materiale del substrato deve possedere diverse caratteristiche fondamentali:
- Resistenza alle alte temperature: Deve resistere a temperature di scarico superiori a 1200°C (2200°F).
- Stabilità termica: Non dovrebbe creparsi o deformarsi sotto l'azione di rapidi sbalzi di temperatura.
- Resistenza strutturale: Deve resistere alle vibrazioni e alle pressioni costanti del sistema di scarico.
- Basso costo: I produttori devono produrlo in modo economico e su larga scala.
Il Washcoat: aumento della superficie reattiva
Il substrato ceramico di per sé non è cataliticamente attivo. Per prepararlo all'assorbimento dei metalli preziosi, i produttori applicano un "washcoat". Si tratta di uno strato di materiale poroso, più comunemente ossido di alluminio (Al₂O₃), applicato sull'intera superficie interna della struttura a nido d'ape.
La funzione del washcoat è quella di aumentare drasticamente la superficie effettiva a livello microscopico. La sua consistenza ruvida e porosa crea innumerevoli anfratti e fessure dove le particelle di catalizzatore possono ancorarsi. Questo aumenta esponenzialmente i siti reattivi disponibili, rendendo il convertitore molto più efficiente rispetto all'applicazione diretta dei metalli sulla ceramica liscia.
I metalli preziosi: la potenza catalitica
Lo strato finale e più cruciale contiene i catalizzatori veri e propri. Si tratta dei metalli preziosi del gruppo del platino: Platino (Pt), Palladio (Pd) e Rodio (Rh)Uno strato molto sottile di questi metalli è legato alla superficie del washcoat.
- Platino (Pt) è un eccellente catalizzatore di ossidazione, altamente efficace nel convertire sia CO che HC.
- Palladio (Pd) funge anche da catalizzatore di ossidazione ed è spesso utilizzato come alternativa più economica o come supplemento al platino.
- Rodio (Rh) è il catalizzatore di riduzione dedicato. Il suo unico scopo è abbattere gli NOx.
L'elevato costo di questi metalli è la ragione principale per cui convertitori catalitici a tre vie Sono preziosi e spesso oggetto di furti. Le case automobilistiche ricercano costantemente nuovi modi per ridurre la quantità di metallo prezioso necessaria (un processo chiamato "thrifting") senza sacrificare l'efficienza di conversione.
Capitolo 4: Le condizioni critiche per prestazioni ottimali
UN convertitore catalitico a tre vie Non funziona al massimo dell'efficienza in tutte le condizioni. Due fattori sono assolutamente cruciali per il suo funzionamento: il rapporto aria-carburante e la temperatura di esercizio. Il sistema di gestione del motore del veicolo è meticolosamente progettato per controllare queste due variabili.
Il rapporto stechiometrico aria-carburante: un delicato equilibrio
Affinché il convertitore esegua efficacemente sia le reazioni di riduzione che quelle di ossidazione, il motore deve funzionare a un rapporto aria-carburante stechiometrico o molto vicino a quello stechiometrico. Per la benzina, questo rapporto è di circa 14,7 parti di aria per 1 parte di carburante in massa (14,7:1).
- Se la miscela è troppo ricca (troppo carburante), non ci sarà abbastanza ossigeno disponibile per ossidare completamente CO e HC.
- Se la miscela è troppo magra (troppa aria), l'ossigeno in eccesso inibirà la riduzione degli NOx, poiché il catalizzatore al rodio non sarà in grado di separare efficacemente l'ossigeno dalle molecole di NOx.
Il “punto debole” per un convertitore catalitico a tre vie Esiste una finestra molto stretta attorno a questo punto stechiometrico. Per mantenere questo equilibrio, i veicoli utilizzano un sistema di feedback a circuito chiuso. I sensori di ossigeno (o sensori O₂) posizionati nel flusso di scarico prima e dopo il convertitore di coppia misurano costantemente il contenuto di ossigeno. Questi dati vengono inviati alla centralina di controllo motore (ECU), che regola in tempo reale l'iniezione di carburante per mantenere il rapporto aria-carburante perfettamente bilanciato.
La temperatura di spegnimento: la necessità di calore
I catalizzatori richiedono una temperatura minima per diventare chimicamente attivi. Questa è nota come temperatura di "accensione", che in genere è compresa tra 250 °C e 300 °C (tra 482 °F e 572 °F). Al di sotto di questa temperatura, il convertitore svolge un'azione molto limitata nella pulizia dei gas di scarico.
Ecco perché le emissioni di un veicolo sono più elevate durante un "avviamento a freddo". Quando il motore si avvia, lo scarico e il convertitore sono freddi. Possono essere necessari diversi minuti di guida prima che il convertitore raggiunga la temperatura di accensione. Durante questa fase di riscaldamento, gli inquinanti non trattati fuoriescono direttamente dal tubo di scarico.
Per contrastare questo problema, gli ingegneri hanno sviluppato diverse strategie:
- Catalizzatori a coppia ravvicinata (CCC): Ciò comporta il posizionamento di un catalizzatore preliminare più piccolo, molto più vicino al collettore di scarico del motore. La vicinanza alla fonte di calore consente di raggiungere la temperatura di spegnimento molto più rapidamente, spesso in meno di 20 secondi.
- Catalizzatori riscaldati elettricamente (EHC): Alcuni sistemi avanzati utilizzano un elemento riscaldante elettrico per preriscaldare il convertitore prima o subito dopo l'avviamento del motore. Questo può ridurre significativamente le emissioni di idrocarburi durante l'avviamento a freddo.
Capitolo 5: Impatto più ampio e applicazioni moderne
IL convertitore catalitico a tre vie È più di un semplice componente di un'auto: è una tecnologia fondamentale per la protezione ambientale globale. La sua diffusa adozione ha contribuito direttamente a una massiccia riduzione dell'inquinamento atmosferico nelle città di tutto il mondo.
Oltre alle normali autovetture, questa tecnologia è adattata a un'ampia gamma di applicazioni che utilizzano motori a combustione interna. Tra queste:
- Camion e autobus
- Motociclette
- Carrelli elevatori e attrezzature minerarie
- generatori elettrici
- Locomotive e imbarcazioni marittime
- Anche alcune stufe a legna avanzate controllano le emissioni di particolato e gas
In ogni caso, i principi fondamentali della catalisi a tre vie vengono adattati per soddisfare normative e condizioni operative specifiche. Il continuo progresso di questa tecnologia è guidato da standard sulle emissioni sempre più severi, come gli standard Euro in Europa e gli standard Tier stabiliti dall'EPA negli Stati Uniti.
Conclusione
IL convertitore catalitico a tre vie è un eroe non celebrato della moderna tecnologia automobilistica. Si tratta di un sofisticato impianto di lavorazione chimica in miniatura, che esegue una complessa danza di reazioni di riduzione e ossidazione. Sfruttando la potenza di platino, palladio e rodio, trasforma un flusso tossico di gas di scarico del motore in gas in gran parte innocui. Il suo sviluppo è stato una risposta diretta ed efficace a una crescente crisi ambientale. Mentre il futuro dei trasporti potrebbe risiedere nei veicoli elettrici, il motore a combustione interna rimarrà prevalente per i decenni a venire. Finché ciò accadrà, il continuo miglioramento e l'applicazione del convertitore catalitico a tre vie saranno essenziali per proteggere l'aria che respiriamo e la salute del nostro pianeta.